执行摘要
子宫内膜异位症(EMT)与子宫内膜息肉(EP)存在显著共患现象,EMT患者中EP的发生率高达47.6%-68.4%,相对危险度达到2.81。两者共享多层面病理机制:分子层面涉及HOXA基因下调、PI3K/AKT/mTOR等信号通路紊乱;细胞层面表现为增殖-凋亡失衡;组织层面包括ECM重塑和血管生成异常;激素层面以ERα高表达和孕激素抵抗为特征;免疫层面涉及NK细胞功能障碍和巨噬细胞极化失衡。
分子机制
HOXA基因表达下调,信号通路交叉调控
细胞层面
增殖优势表型,凋亡抵抗机制
组织重塑
ECM重构异常,血管生成活跃
临床诊治中的核心迷思包括因果关系的"鸡生蛋"困境、诊断技术的局限性、药物与手术的权衡、以及复发风险的长期管理。整合两种疾病的共同机制进行靶向干预,是未来精准诊疗的方向。
疾病概述与流行病学关联
子宫内膜异位症特征
定义
具有活性的子宫内膜腺体和间质组织出现在子宫腔被覆黏膜及宫体肌层以外的部位
分型
- • 卵巢型(巧克力囊肿)
- • 腹膜型(盆腔表面病灶)
- • 深部浸润型(DIE,浸润≥5mm)
子宫内膜息肉特征
定义
由子宫内膜局部腺体和间质过度增生形成的良性病变,具有纤维血管轴心
分型
- • 有蒂型(细长蒂部连接)
- • 无蒂型(广基附着)
- • 功能性/非功能性息肉
共患病流行病学证据
| 研究类型 | EMT患者EP发生率 | 对照组发生率 | 效应量 |
|---|---|---|---|
| Meta分析 | 47.6%-68.4% | 7.8%-34.9% | RR=2.81 (2.48-3.18) |
| 前瞻性队列 | 46.7% | 16.5% | OR≈4.2 |
数据来源:Gui et al., 2015
共同发病机制的多层面解析
分子生物学机制
HOXA基因家族调控
HOXA10/HOXA11表达下调
在EMT和EP中表达降低40-60%,影响子宫内膜容受性
表观遗传修饰
DNA甲基化、组蛋白修饰和非编码RNA调控共同参与
信号通路交叉调控
关键信号通路紊乱
| 信号通路 | 核心分子改变 | EMT主要效应 | EP主要效应 |
|---|---|---|---|
| PI3K/AKT/mTOR | p-AKT↑、mTORC1活性↑ | 异位细胞存活、代谢重编程 | 增殖增强、凋亡抑制 |
| Wnt/β-catenin | 核β-catenin↑、TCF/LEF活性↑ | 干细胞维持、侵袭性 | 上皮祖细胞扩增 |
| TGF-β/Smad | TGF-β1↑、p-Smad2/3↑ | 纤维化粘连、免疫抑制 | 基质硬化、血管重塑 |
细胞层面机制
增殖-凋亡失衡
- • Ki-67指数升高30-50%
- • Bcl-2高表达,凋亡指数降低
- • PI/AI比值 > 3.0
干细胞分化异常
- • 子宫内膜干细胞活化
- • 间充质干细胞分化偏倚
- • EMT过程协同调控
细胞周期紊乱
- • Cyclin D1过表达
- • CDK4/6活性增强
- • G1期缩短,S期加速
分子标志物表达特征
| 分子标志物 | EMT患者EP | 非EMT患者EP | 临床意义 |
|---|---|---|---|
| Bcl-2 | +++ (显著升高) | ++ (中等表达) | 预测复发风险、指导治疗 |
| ERα | +++ (显著升高) | ++ (中等表达) | 激素治疗敏感性标志 |
| Ki-67 | 25-35% | 15-20% | 增殖活性评估 |
| PI/AI比值 | >3.0 | 1.5-2.5 | 综合风险评估 |
组织层面机制
细胞外基质重塑
MMPs系统活化
MMP-2/9活性升高2-5倍,MMP-7表达突出,TIMPs相对不足
胶原沉积异常
I/III型胶原比例改变,组织硬化,弹性下降
整合素信号
α5β1等受体上调,提供细胞存活信号
血管生成与微环境
VEGF信号
VEGF高表达,与病灶血管密度和出血倾向相关
PROK1/PROKR1轴
PROKR1表达升高8.66倍,受体亚型失衡
HIF-1α调控
缺氧适应反应,促进血管生成因子转录
激素调控网络异常
雌激素信号
- • ERα高表达,敏感性增强
- • 局部芳香化酶活性增高
- • 自分泌雌激素微环境
孕激素抵抗
- • PR-B表达下调
- • PR-A/PR-B比值升高
- • 下游信号传导障碍
免疫系统失调
先天免疫异常
- • NK细胞功能缺陷
- • 巨噬细胞M2极化
- • SIRPα表达升高
适应性免疫紊乱
- • Th1/Th2平衡偏移
- • Th17细胞过度活化
- • Treg功能异常
两种疾病因果关系的临床判断迷思
"鸡生蛋还是蛋生鸡"的困境
EMT先于EP
EMT系统性因素影响在位内膜,使其呈现息肉前表型
DIE与EP关联更强,解剖位置支持因果影响
新诊断EMT患者内膜活检已见息肉前改变
EP先于EMT
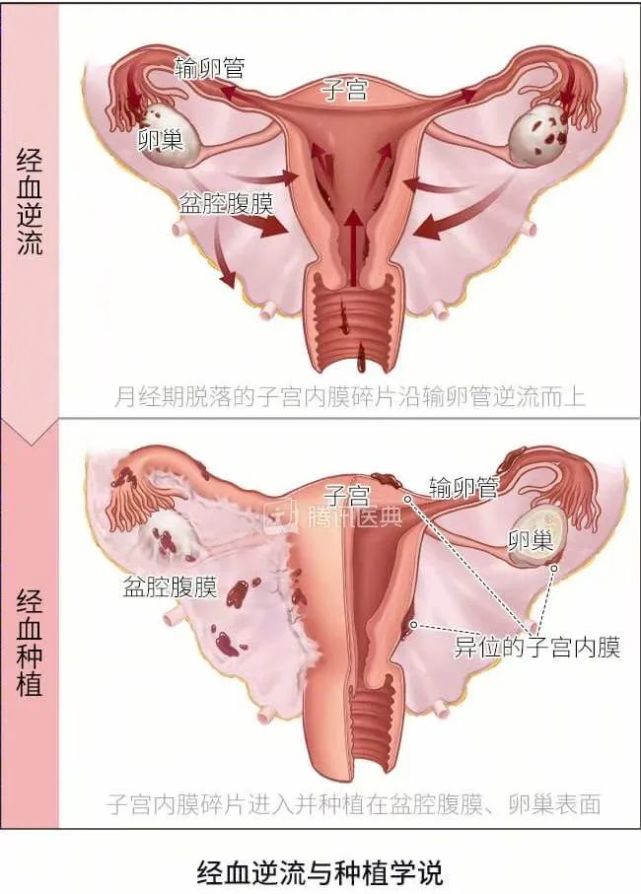
EP慢性炎症因子经输卵管逆流,改变腹膜微环境
占位病变导致宫腔环境改变,促进经血逆流
宫腔镜等操作存在内膜细胞腹腔种植理论风险
平行发生
WNT4、GREB1等基因位点与两种疾病均相关
初潮早、周期短、经量多等共同危险因素
长期无孕激素对抗的雌激素暴露同时促进两种疾病
因果推断的方法学挑战
观察性研究的固有局限
横断面研究
无法确定时序关系,因果推断能力弱
回顾性研究
受回忆偏倚、选择偏倚影响
选择偏倚
不孕中心人群EMT和EP检出率均高
潜在混杂因素控制
年龄因素
两种疾病发病率随年龄变化模式不同
BMI影响
通过雌激素代谢和炎症状态影响两种疾病
合并疾病
PCOS、子宫腺肌病等共同合并症
解决方案需求
需要大规模、前瞻性、长期随访的队列研究,以及利用遗传工具变量等因果推断方法的创新设计,才能准确判断EMT与EP的因果关系。
诊断标准与方法的局限性
诊断技术的敏感性与特异性
经阴道超声(TVS)
EP诊断性能
敏感性70-90%,特异性80-95%
EMT诊断性能
卵巢型>90%,腹膜型<50%< /p>
主要局限
操作者依赖,小病变易漏诊
MRI成像
EP诊断性能
敏感性60-80%(大小相关)
EMT诊断性能
DIE敏感性85-95%
主要局限
费用高,小型EP易漏诊
宫腔镜检查
EP诊断
金标准,直视下活检
EMT评估
微小病灶易漏诊,宫腔外无法观察
主要局限
侵入性操作,存在并发症风险
"金标准"的地位与盲区
宫腔镜检查的盲区
微小EMT病灶漏诊
腹膜型EMT位于子宫外,宫腔镜无法评估
镜下鉴别困难
内膜炎与早期EMT表现相似,易混淆
活检代表性问题
单点活检可能遗漏局灶性病变
腹腔镜的诊断价值
EMT确诊金标准
直接观察盆腔病灶,进行准确分期
EP评估盲区
无法直接观察宫腔内病变
应用限制
设备、技术、费用等因素限制
病理诊断的标准化问题
EP病理诊断挑战
- • 腺体与间质比例判定缺乏统一标准
- • 息肉样增生与真性息肉区分困难
- • 不典型增生识别存在观察者间差异
- • WHO分类应用仍需实践经验
EMT病理确诊标准
- • 三联征:腺体+间质+含铁血黄素
- • 部分特征病例需结合临床
- • 不典型EMT识别需要高度警觉
- • 免疫组化(CD10, ER/PR)辅助价值
合并病变报告规范
- • 同步描述EP和EMT组织学特征
- • 寻找两者间组织学联系
- • 分子标志物检测建议
- • 提供预后信息和治疗指导
治疗方案的选择与权衡迷思
药物治疗 vs 手术治疗的决策困境
药物治疗选择比较
| 药物类别 | EP适应证 | EMT适应证 | 主要优势 | 主要局限 |
|---|---|---|---|---|
| 口服孕激素 | 有症状、术前准备 | 疼痛控制、病灶抑制 | 灵活调整、可逆 | 突破性出血、依从性 |
| LNG-IUS | 术后预防复发首选 | 痛经、轻-中度病变 | 局部高效、全身副作用小 | 放置操作、初期出血 |
| GnRH-a | 术前缩瘤 | 中重度、术前/术后 | 快速降雌激素、疗效确切 | 低雌激素症状、骨丢失 |
药物治疗局限性
孕激素抵抗
ERα高表达、PR低表达者反应不佳,常规检测尚未普及
GnRH-a副作用
低雌激素症状显著,骨丢失风险限制长期应用
依从性问题
长期用药患者接受度下降,影响治疗效果
手术治疗考量
EP切除技术选择
电切术 vs 冷刀刨削系统,后者妊娠率更高、复发率更低
EMT手术决策
囊肿剥除 vs 附件切除,需权衡生育力与复发风险
联合治疗序列
"药物预处理-手术-药物维持"模式最优化
保守治疗 vs 根治性治疗的年龄与生育考量
育龄期患者
核心矛盾:生育力保护与疾病控制的平衡
保守手术:复发率较高(EMT 20-40%,EP 15-30%),但保留生育功能
妊娠窗口:术后6-12个月未孕建议积极转向ART
反复流产:需综合评估EMT和EP对妊娠结局的影响
围绝经期患者
特殊阶段:激素波动加剧症状,但自然缓解预期
治疗强度:症状严重者需积极干预,可控者可适度保守
恶变监测:EMT卵巢恶变风险约1%,EP恶变率<3%< /p>
最后窗口:需个体化决策,权衡治疗强度
根治性手术
指征把握:药物治疗失败、症状严重影响生活质量
卵巢决策:保留 vs 切除,影响激素状态和长期健康
患者参与:生活质量与疾病控制的共同决策
多学科协作:涉及肠道、泌尿系时需MDT
特殊临床情境的治疗迷思
无症状EP合并EMT的管理
期待治疗条件:息肉<1cm、无不孕史、无恶变高危因素< /p>
随访策略:6-12个月复查超声,个体化监测
避免过度治疗:医患共同决策,平衡风险与获益
复发性EP合并EMT的策略
复发风险:2.5%-43.6%,合并EMT者更高
内膜损伤累积:多次手术可能导致宫腔粘连
分子标志物:Bcl-2、Ki-67检测指导强化治疗
ART前的预处理
息肉切除价值:妊娠率提高15-20%
EMT手术影响:卵巢手术可能减少卵巢储备
策略选择:优先IVF vs 延迟EMT手术的权衡
关键决策要点
- • 个体化评估患者年龄、生育需求
- • 平衡治疗效果与生活质量
- • 充分考虑患者偏好与依从性
- • 建立长期管理规划
复发风险与长期管理策略
复发风险的预测模型
EP复发危险因素
高危因素
- • 多发息肉 (OR=9.50)
- • 直径>2cm
- • 术后内膜厚>10mm (OR=1.32)
- • EMT合并存在
- • PCOS史 (OR=47.20)
中危因素
- • 年龄>45岁
- • BMI>30 (OR=1.29)
- • 未绝经状态
- • 剖宫产史 (OR=9.27)
EMT复发危险因素
疾病相关
- • 高分期(III-IV期)
- • 卵巢型病灶
- • 深部浸润型(DIE)
- • 初次手术不彻底
治疗相关
- • 术后药物维持依从性差
- • 家族史阳性
- • 遗传易感因素
共患病协同效应
机制协同
- • 共同分子通路激活
- • 炎症微环境维持
- • 激素调控网络紊乱
管理启示
- • 单一疾病控制不足
- • 需整合管理策略
- • 共同靶点干预价值
术后药物辅助治疗的证据
LNG-IUS策略
术后即刻放置:时机优势,无缝衔接手术效果
5年续用率:约60%-80%,主要停用原因:不规则出血
月经模式管理:充分告知,提高接受度
首选推荐:术后预防复发的首选方案
COC长期管理
连续服用:vs 周期服用,症状控制更佳
风险评估:35岁以上、吸烟、血栓史需谨慎
依从性优势:口服给药,患者接受度高
成本效益:相对经济的治疗选择
GnRH-a间歇应用
短期强化:3-6个月,清除残留病灶
长期间歇:每6个月1-3个月疗程
骨保护策略:基线及年度DXA监测
营养补充:钙剂1000mg/日+维生素D 800-1000IU/日
生活方式与代谢干预
体重管理
目标BMI:18.5-23.9 kg/m²
减重目标:5%-10%体重
减重速度:每周0.5-1kg
机制:降低芳香化酶活性,改善激素平衡
饮食营养
抗炎饮食:地中海饮食模式
营养素补充:维生素D >30 ng/mL
Omega-3:EPA/DHA抗炎作用
限制食品:红肉、加工食品、高糖食物
运动压力
适度运动:每周150分钟中等强度
避免过度:防止下丘脑性闭经
压力管理:正念、瑜伽、CBT
综合益处:改善代谢、调节免疫
随访监测的个体化方案
影像学随访策略
基线评估
术后3-6个月经阴道超声,记录内膜厚度、回声特征、血流信号
风险分层随访
- • 低危:每年1次
- • 中危:每6个月1次
- • 高危:每3个月1次
补充检查
超声可疑复发时,MRI提供更详细解剖信息,尤其适用于DIE评估
症状监测与教育
AUB复发识别
- • 经量增多、经期延长
- • 经间期出血
- • 异常出血模式改变
痛经模式警示
- • 疼痛程度加重
- • 疼痛时间延长
- • 非周期性疼痛出现
PROMs工具应用
疼痛视觉模拟评分、生活质量问卷等量化工变化
生育计划整合
孕前咨询:疾病稳定后3-6个月,评估疾病对妊娠影响
妊娠期监测:以症状为主,多数患者妊娠期症状改善
产后预防:利用哺乳期自然避孕,规划后续药物维持
未来研究方向与临床转化
机制研究的深化
单细胞测序技术
解析EMT和EP组织的细胞异质性
识别关键的致病细胞亚群
揭示细胞通讯网络
追踪状态转换轨迹
类器官模型
患者来源三维培养体系
模拟疾病微环境
机制研究和药物筛选
弥补二维培养局限
多组学整合
基因组、转录组、蛋白质组
代谢组、表观基因组
构建全面调控网络
识别核心干预靶点
精准诊疗的探索
分子分型指导治疗
分型标志物
- • ER/PR表达谱
- • 增殖指数(Ki-67)
- • 凋亡标志物(Bcl-2/Bax)
- • 信号通路活化状态
预测价值
- • 治疗方案反应性预测
- • 药物选择和剂量优化
- • 复发风险评估
- • 个体化治疗决策
新型靶向药物
抗血管生成药物
贝伐珠单抗等,抑制VEGF信号通路
免疫调节药物
PD-1/PD-L1抑制剂,调节免疫微环境
信号通路抑制剂
PI3K/AKT/mTOR、Wnt/β-catenin等小分子抑制剂
临床研究的优化设计
前瞻性队列研究
- • 建立大规模长期随访队列
- • 提供疾病自然史真实世界数据
- • 识别危险因素效应和预后因子
- • 弥补回顾性研究局限
随机对照试验
- • 息肉切除对IVF结局影响
- • 术后药物维持最优方案
- • 不同分子亚型治疗反应差异
- • 为指南更新提供高级别证据
真实世界数据
- • 系统收集复杂临床情境数据
- • 补充传统临床试验不足
- • 反映实际治疗效果
- • 加速研究成果临床转化
未来愿景
整合两种疾病的共同机制进行靶向干预,是未来精准诊疗的方向。从"分病而治"转向"同治共病",需要临床医师超越传统专科界限,建立系统性的疾病管理思维,最终实现改善患者预后和生活质量的核心目标。