卵巢纤维化诱发卵巢早衰的
病理机制及治疗新策略
基于香港大学Science突破性研究的抗纤维化药物治疗证据
关键突破
核心发现
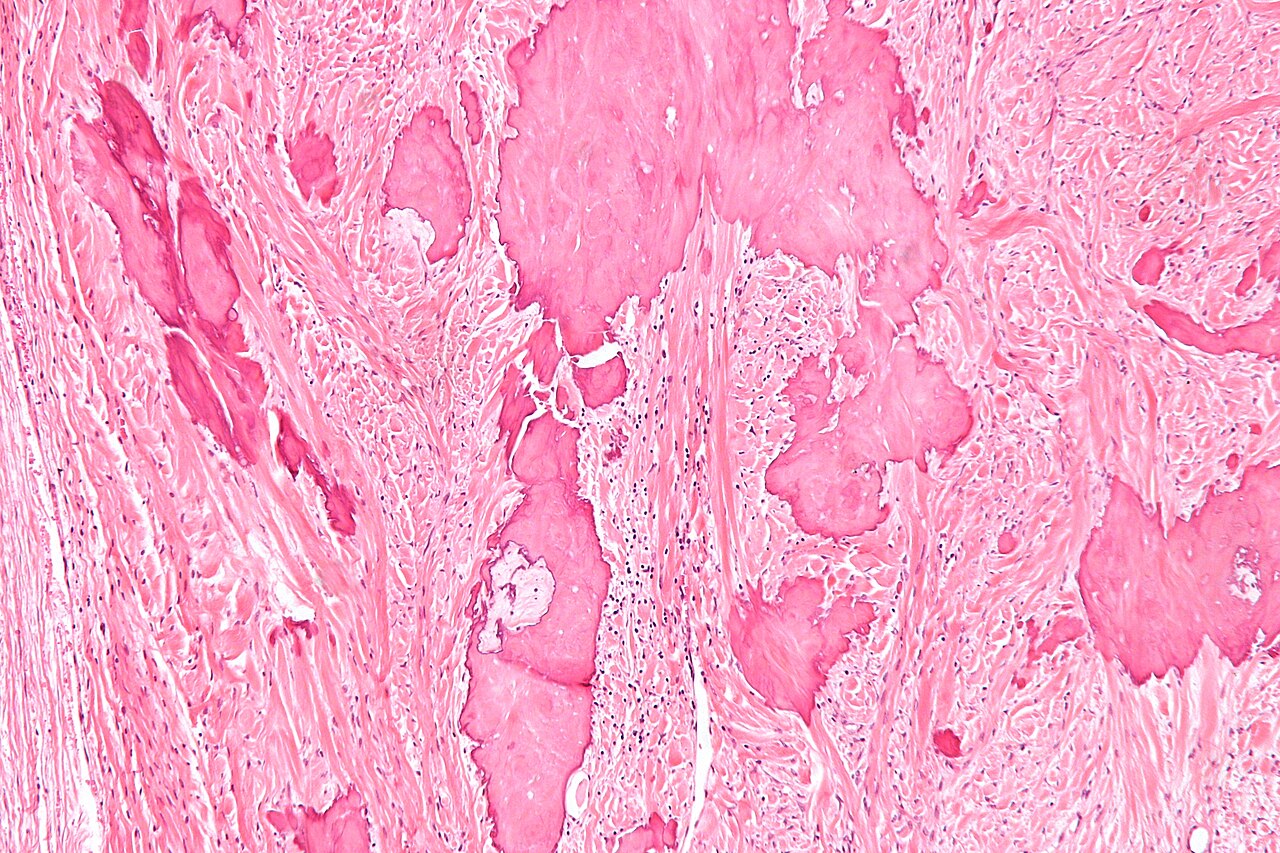
卵巢纤维化通过细胞外基质过度沉积、基质硬化及信号通路紊乱破坏卵泡发育微环境,导致卵泡激活障碍和卵巢功能衰竭。2026年2月香港大学团队在Science发表的研究证实,非奈利酮(Finerenone)等抗纤维化药物可逆转这一过程。
在14例常规治疗无效的POI患者中,经治疗后100%恢复卵泡发育,约50%获得成熟卵母细胞,标志着POI治疗从"直接刺激卵泡"向"改善卵巢微环境"的范式转变。
临床意义
卵巢纤维化的病理生理机制
定义与特征
核心信号通路异常
TGF-β/Smad信号通路:纤维化的核心枢纽
TGF-β1过度表达
老年小鼠卵巢中TGF-β1 mRNA水平升高约40%,直接刺激ECM合成
Smad复合物激活
Smad2/3磷酸化后与Smad4形成复合物,激活Col1a1等纤维化基因
EMT促进
诱导上皮细胞向间质转化,增加肌成纤维细胞来源
ECM稳态失衡机制
MMP活性降低
基质金属蛋白酶活性普遍下降,胶原纤维降解不足
TIMP表达升高
组织金属蛋白酶抑制物表达上调,抑制ECM降解
比例失调
MMP/TIMP比例发生显著逆转,ECM降解全面受阻
关键发现:间充质干细胞治疗通过上调TIMP-1、下调MMP-9,减轻纤维化程度,提示MMP/TIMP平衡的恢复是抗纤维化治疗的重要机制 [71]。
卵巢纤维化诱发卵巢早衰的具体病理过程
卵泡发育微环境破坏
基质硬化限制卵泡扩张
卵泡发育伴随显著的体积增大:从原始卵泡(直径约30μm)到成熟卵泡(直径可达20-25mm),体积增加超过百万倍。纤维化导致的基质硬化使卵巢组织弹性模量显著增加 [95]。
- • 原子力显微镜:衰老卵巢弹性模量增加2-3倍
- • 基质刚度>5-10 kPa抑制颗粒细胞增殖
- • 机械应力激活YAP/TAZ通路
- • 严重时可触发卵泡闭锁程序
卵泡发育停滞的关键环节
卵巢内分泌功能损害
颗粒细胞功能受抑
颗粒细胞是卵泡内分泌功能的核心执行者,负责雌激素合成和卵泡液成分调控。纤维化微环境通过多重机制抑制颗粒细胞功能。
- • 硬化基质激活YAP/TAZ通路,抑制增殖
- • 缺氧诱导HIF-1α持续激活,干扰代谢
- • 炎症因子直接抑制芳香化酶活性
- • 营养供应不足影响合成功能
雌激素合成减少
卵巢纤维化导致的颗粒细胞功能障碍和卵泡发育停滞,直接造成雌激素合成显著减少,引起一系列低雌激素症状。
- • 月经稀发或闭经
- • 血管舒缩症状
- • 生殖道萎缩
- • 骨密度下降
- • 芳香化酶活性抑制
- • 雄激素底物不足
- • 卵泡数量减少
- • 负反馈失调
抗纤维化药物治疗卵巢早衰的临床证据
非奈利酮(Finerenone)突破性临床试验
研究设计与患者特征

主要临床结局数据
| 结局指标 | 结果 | 临床意义 |
|---|---|---|
| 卵泡发育恢复率 | 100%(14/14例) | 所有患者均恢复卵泡发育,远超传统治疗预期 |
| 优势卵泡发育 | 57%(8/14例) | 卵泡发育可完成关键阶段,获得排卵潜能 |
| 成熟卵子获取率 | 约50%(7/14例) | POI人群中极为罕见的获卵率 |
| 可移植胚胎 | 3个(5例患者) | 实现治疗终极目标——产生可用胚胎 |
| 卵母细胞冷冻 | 3例患者 | 为延迟生育保留自体卵子选项 |
其他FDA批准抗纤维化药物的临床前证据
抗纤维化药物谱系比较
尼达尼布
芦可替尼
吡非尼酮
非奈利酮
抗纤维化药物治疗卵巢早衰的动物实验证据
衰老小鼠模型研究
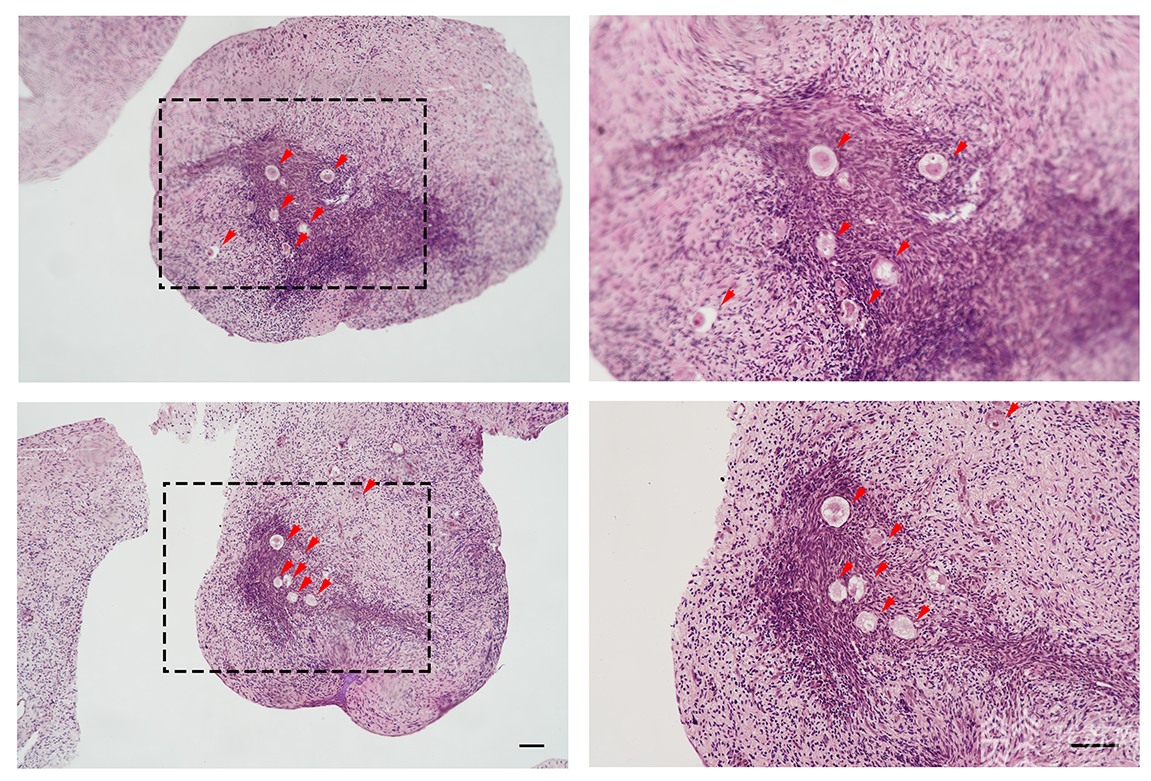
模型建立
非奈利酮干预效果
机制验证实验
组织学分析
抗纤维化药物治疗卵巢早衰的基础研究机制
核心治疗靶点的范式转变
治疗策略对比
| 方面 | 传统策略 | 新策略 |
|---|---|---|
| 治疗靶点 | 卵泡本身 | 卵巢微环境(基质纤维化) |
| 获益人群 | 卵巢储备尚可者 | 包括传统治疗无效的严重POI患者 |
| 药物选择 | 促性腺激素等有限选项 | 多种抗纤维化药物,机制互补 |
| 安全性 | 过度刺激风险 | 改善微环境,更温和 |
| 与ART整合 | 强制刺激方案 | 微环境改善后自然周期或轻微刺激 |
非奈利酮的具体作用机制
核心机制:阻断盐皮质激素受体(MR)
高选择性MR拮抗剂,阻断卵巢间质细胞中过度激活的MR信号
抗纤维化效应:从分子到组织
其他抗纤维化药物的机制差异
不同靶点的汇聚效应
共同机制特征
卵巢纤维化相关危险因素与特殊人群
医源性因素
内分泌代谢因素
临床启示
识别卵巢纤维化的危险因素对于POI的预防和治疗具有重要意义。特别是对于具有医源性、内分泌或免疫相关风险因素的女性,早期干预可能有助于减缓纤维化进程,保护卵巢功能。
研究局限性与未来方向
当前证据的局限性
研究发展路线图
概念验证
已完成:n=14探索性临床试验
确证研究
进行中:多中心RCT设计
优化应用
规划中:方案个体化
临床转化
目标:专科门诊建设