妊娠期糖尿病
药物治疗选择
的深度研究
基于循证医学证据的临床决策框架与未来发展方向
胰岛素首选地位
不通过胎盘屏障,对胎儿无直接暴露风险,全球指南一致推荐
口服药替代选择
二甲双胍可作为胰岛素替代,但需注意胎盘透过性
格列本脲争议
因安全性争议,临床使用趋于谨慎
新型药物探索
GLP-1受体激动剂等新兴药物尚缺乏妊娠期安全性数据

1. 临床一线治疗方案:胰岛素治疗
1.1 胰岛素作为首选药物的理论基础
胎盘屏障特性与不通过胎盘的优势
胰岛素作为大分子蛋白质激素,分子量约为5808道尔顿,这一物理化学特性决定了其无法通过胎盘屏障。胎盘屏障对分子物质的通透性具有严格选择性,通常分子量大于1000道尔顿的物质难以自由通过胎盘绒毛膜[71] [70]。
这一独特的药理学特性构成了胰岛素在妊娠期糖尿病治疗中核心地位的基石——与口服降糖药不同,胰岛素不会直接进入胎儿血液循环,因此不会对胎儿胰腺β细胞的发育和功能产生直接刺激作用,也不会导致胎儿高胰岛素血症的发生。
胎儿保护原则
胰岛素治疗完全规避了胎儿高胰岛素血症风险,其降糖作用仅限于母体,通过控制母体血糖间接改善胎儿宫内环境,而非直接干预胎儿代谢。这一作用模式符合妊娠期用药的"胎儿保护原则",即在有效治疗母体疾病的同时,最大限度减少药物对胎儿的直接影响[52] [70]。
全球指南一致推荐地位
胰岛素在全球妊娠期糖尿病治疗指南中享有无可争议的首选地位。美国糖尿病学会(ADA)2023年"妊娠合并糖尿病诊治指南"明确指出,胰岛素是治疗GDM的首选药物,证据等级为A级 [101]。
1.2 胰岛素治疗方案的具体实施
基础-餐时强化治疗方案
1.3 新型胰岛素类似物的临床应用进展
甘精胰岛素U300的最新推荐
2024版中国指南重要更新
2024版《中国糖尿病防治指南》将甘精胰岛素U300新增为妊娠期基础胰岛素的治疗选择[52] [67] [68]。
- 药物说明书包含妊娠期使用信息
- 上市后循证医学证据积累
- 国际临床实践数据支持
- 更平稳的作用曲线
- 更低的夜间低血糖风险
- 更持久的药效覆盖
真实世界研究证据
2026年发表的一项印度多中心回顾性真实世界研究纳入132名在怀孕前开始使用甘精胰岛素U300治疗的妊娠期糖尿病患者[58]。
德谷胰岛素的应用现状
EXPECT研究里程碑
EXPECT研究是一项里程碑式的国际多中心随机对照试验,纳入225例1型糖尿病孕妇,结果显示德谷胰岛素与地特胰岛素在血糖控制效果和安全性方面达到非劣效性标准 [73]。
注意:该研究主要针对1型糖尿病孕妇,GDM患者仅占少数,证据外推需谨慎。
1.4 胰岛素治疗的挑战与患者管理
注射负担
- 每日多次注射(通常4次/日)
- 注射疼痛与皮肤反应
- 生活方式干扰
- 心理"疾病标签"效应
低血糖风险
- 定义:血糖<3.3 mmol/L
- 严重低血糖需他人协助
- 夜间低血糖风险
- 需要紧急处理预案
体重增加
- 胰岛素促进合成代谢
- 妊娠期生理性体重增加
- 需要营养与运动配合
- 避免过度治疗
2. 口服降糖药在GDM中的应用现状
2.1 二甲双胍的临床应用与证据
作用机制与优势
二甲双胍主要通过激活AMP活化蛋白激酶(AMPK)信号通路,实现多靶点的代谢调节效应:在肝脏,抑制糖异生关键酶的表达和活性,减少肝糖输出;在外周组织,增强胰岛素受体后信号传导,提高胰岛素敏感性[48] [79]。
临床优势
- • 不刺激胰岛β细胞分泌胰岛素
- • 单独使用时低血糖风险极低
- • 具有轻度减重作用
- • 口服给药,患者依从性好
里程碑式研究:MiG试验
长期随访研究:MiG TOFU
9年随访结果显示,二甲双胍暴露组与胰岛素暴露组后代在体重指数(BMI)、腰围、血糖代谢指标、胰岛素敏感性等方面无显著差异 [102]。
这一发现对于评估二甲双胍对胎儿代谢编程的潜在影响至关重要,表明宫内二甲双胍暴露未对后代的长期代谢健康产生明显不良影响。
2.2 格列本脲的临床应用与争议
安全性争议核心
3. 新兴药物与潜在治疗方向
3.1 GLP-1受体激动剂的研究进展
作用机制与潜在优势
GLP-1受体激动剂模拟天然GLP-1的作用,其降糖作用具有葡萄糖依赖性特征:在高血糖状态下促进胰岛素分泌、抑制胰高血糖素释放;在血糖正常或低血糖状态下,这一作用减弱或消失[36]。
固有的低血糖安全性,提供"宽容"的治疗窗口
延缓胃排空、抑制食欲,对超重患者有额外价值
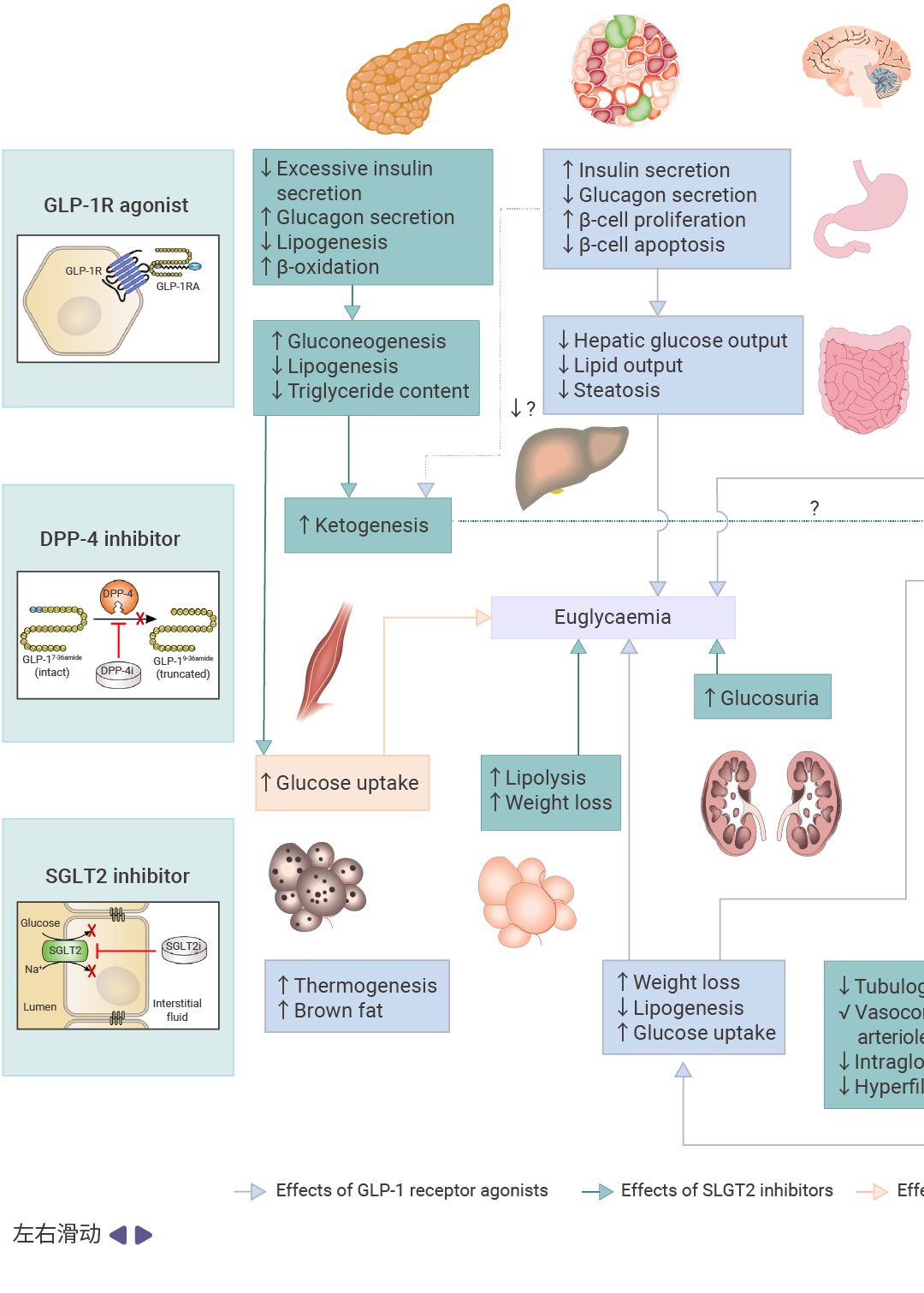
当前安全性信号
动物实验发现
- • 胎儿生长迟缓
- • 骨骼异常
- • 胎儿丢失率增加
人类数据现状
- • 人类妊娠期数据极为有限
- • 药品说明书均列为禁忌
- • 英国MHRA发布紧急警报[36]
2023年Meta分析结果
JAMA Internal Medicine发表的Meta分析整合北欧、美国和以色列6个大型医疗数据库,纳入938例围孕期GLP-1受体激动剂暴露的妊娠[35]。
3.2 SGLT2抑制剂的探索性研究
妊娠期生理适应性挑战
肾脏生理变化
- • 肾血流量增加30%-50%
- • 肾小球滤过率显著增加
- • 生理性糖尿已存在
- • 容量丢失风险加剧
安全性担忧
- • 电解质紊乱风险增加
- • 正常血糖性糖尿病酮症酸中毒
- • 妊娠期已存在生理性酮症倾向
- • 胎儿营养供应担忧
2026年韩国队列研究发现
韩国全国性出生队列研究纳入121例孕早期SGLT2抑制剂暴露和2,007例胰岛素暴露的妊娠[39]。
器官形成期(孕4-10周)暴露的先天性心脏缺陷风险升高至2.79(95%CI 1.16-7.06)
3.3 其他潜在药物类别
DPP-4抑制剂
噻唑烷二酮类药物
4. 药物治疗决策的临床考量
4.1 患者分层与个体化选择
血糖升高类型与药物匹配策略
空腹血糖升高为主
餐后血糖升高为主
空腹及餐后均升高
个体化决策考量因素
患者相关因素
- • 血糖升高模式分析
- • 治疗偏好与依从性评估
- • 经济条件与保险覆盖
- • 教育水平与自我管理能力
医疗系统因素
- • 医疗资源可及性
- • 专业团队支持能力
- • 随访监测条件
- • 低血糖应急处理能力
4.2 特殊人群的用药考量
孕前已使用口服降糖药患者的管理
计划妊娠
- • 孕前咨询讨论药物转换
- • 确认妊娠后即转换为胰岛素
- • 规避早期胚胎暴露风险
意外妊娠
- • 详细药物暴露评估
- • 二甲双胍:加强胎儿监测
- • 格列本脲:谨慎评估风险
多囊卵巢综合征合并GDM患者
PCOS患者是GDM的高危人群,其病理生理特征(胰岛素抵抗、高胰岛素血症、肥胖)与GDM高度重叠。二甲双胍在PCOS患者中的应用历史悠久,许多患者在孕前已长期使用该药[48]。
管理策略
• 改善胰岛素敏感性
• 减少体重增加
• 可能降低流产风险
• 消除胎儿暴露不确定性
• 更精确的血糖控制
• 避免胎盘透过风险
4.3 多学科协作管理模式
协作管理核心要素
专业协作
- • 内分泌科与产科联合随访
- • 定期多学科团队会议
- • 共享决策信息平台
- • 紧急联络机制
综合干预
- • 药物治疗与生活方式结合
- • 营养支持个性化调整
- • 运动处方安全实施
- • 心理健康支持
5. 未来研究方向与未满足需求
长期安全性随访
- • 青春期发育影响
- • 成年期糖代谢结局
- • 心血管风险预测
- • 神经发育评估
- • 国际协作暴露登记数据库
- • 多中心长期队列研究
- • 子代生殖健康监测
新型药物注册试验
- • 德谷胰岛素妊娠期数据
- • 甘精胰岛素U300扩展研究
- • 新型速效胰岛素类似物
- • 妊娠期特异性药代动力学
- • 非劣效性比较设计
- • 全面母婴安全性评估
精准医学指导下的个体化用药
结论与展望
核心观点总结
胰岛素仍是首选
基于不通过胎盘屏障的独特优势,全球指南一致推荐胰岛素作为GDM一线治疗药物,确保对胎儿的最大程度保护。
口服药替代选择
二甲双胍可作为胰岛素替代选择,尤其在体重控制和新生儿低血糖风险方面具有优势,但需注意胎盘透过性及中国尚未批准妊娠期适应证。
格列本脲趋于谨慎
因安全性争议,特别是新生儿不良结局风险,格列本脲的临床应用趋于谨慎,不再是首选口服药物。
未来发展方向
新型胰岛素优化
甘精胰岛素U300、德谷胰岛素等新型胰岛素类似物的妊娠期应用证据不断积累,为临床提供更多安全有效的治疗选择。
精准医学应用
药物基因组学和多组学数据分析将推动GDM治疗向个体化、精准化方向发展,实现最优治疗效果。
证据体系完善
建立国际协作的妊娠期暴露登记数据库,加速真实世界证据积累,为指南更新和临床决策提供坚实基础。
"妊娠期糖尿病的药物治疗需要在疗效、安全性和个体化需求之间找到最佳平衡点,这不仅关乎母亲的健康,更影响着下一代的终身福祉。"
基于循证医学的个体化治疗策略,结合多学科协作管理,将为GDM患者带来更好的临床结局和生活质量。