NAD+抗衰老治疗
对试管婴儿治疗的影响
机制、阶段效应与补充方式比较
科学前沿
基于细胞能量代谢、DNA修复和表观遗传调控的分子机制, 探索NAD+补充在辅助生殖技术中的应用潜力与临床证据。
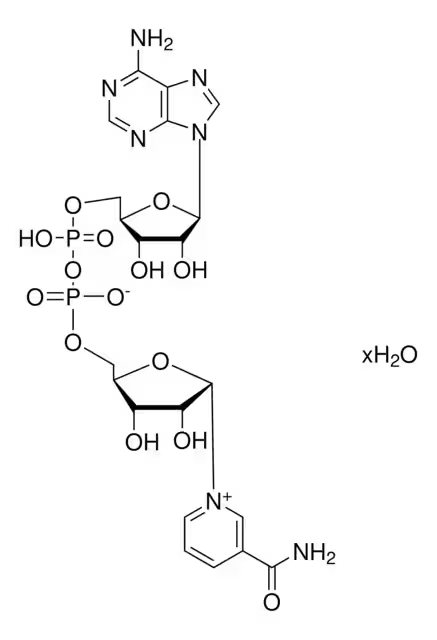
NAD+分子结构
执行摘要
核心发现
NAD+补充对试管婴儿治疗具有潜在帮助,尤其针对卵巢储备功能下降、高龄或既往反应不佳的患者。 其核心机制在于改善线粒体能量代谢、增强DNA修复能力、优化表观遗传调控和减轻氧化应激, 从而在卵子成熟、受精、胚胎发育等多个阶段产生积极影响。
现有临床证据显示,静脉注射NAD+可使成熟卵子数量增加约50%,优质胚胎数量增加一倍以上 [114]。 恩艾地注射剂作为中国首个获批的NAD+静脉制剂,具有近乎100%的生物利用度和快速起效优势, 但成本较高且需医疗场所给药;口服前体(NMN、NR)则更适合长期维持。
生物学机制
- • 线粒体ATP产生优化
- • DNA修复酶PARP激活
- • Sirtuin表观遗传调控
- • 氧化应激防御增强
临床证据
- • 112例自身对照研究
- • 卵巢低反应患者群体
- • 澳大利亚RCT进行中
- • 动物实验活产率改善
补充策略
- • 静脉注射:快速起效
- • 口服前体:长期维持
- • 序贯联合应用
- • 个体化剂量调整
1. NAD+的生物学基础与生殖衰老机制
1.1 NAD+的核心生物学功能
细胞能量代谢
NAD+(烟酰胺腺嘌呤二核苷酸)是细胞内最核心的代谢辅酶之一,其氧化还原功能直接驱动线粒体ATP的产生。 在卵母细胞这一特殊细胞类型中,NAD+的作用被放大至极致—— 人类卵母细胞是人体最大的单细胞,直径约100-120微米,却仅含有约10万个线粒体 [122], 这一"能量贫困"状态使其对NAD+介导的氧化磷酸化效率极为敏感。
关键机制:NAD+作为电子传递链复合物I的关键底物, 接受来自三羧酸循环的电子形成NADH,随后驱动质子梯度建立和ATP合酶活性。
DNA修复与基因组稳定性
NAD+在DNA修复网络中扮演多重角色,这一功能对生殖细胞尤为重要。 PARP(聚ADP核糖聚合酶)家族酶以NAD+为唯一底物 [126], 在DNA单链断裂修复中发挥核心作用。
关键机制:当DNA损伤发生时,PARP1被激活并消耗大量NAD+合成PAR链, 招募XRCC1、DNA连接酶III等修复蛋白至损伤位点。
NAD+在卵母细胞中的代谢通路
1.2 生殖衰老中的NAD+耗竭机制
卵巢NAD+水平随年龄下降的病理生理
女性生殖衰老呈现加速特征,35岁后生育力急剧下降,40岁后自然妊娠率低于5%, 这一时间窗口与卵巢NAD+水平的显著降低高度吻合。2023年《Aging Cell》发表的研究揭示, 中年小鼠(8-12月龄)卵巢中NAD+从头合成关键酶Ido1和Qprt的表达显著下降 [135], 导致NAD+水平较年轻个体(3月龄)降低30%-50%。
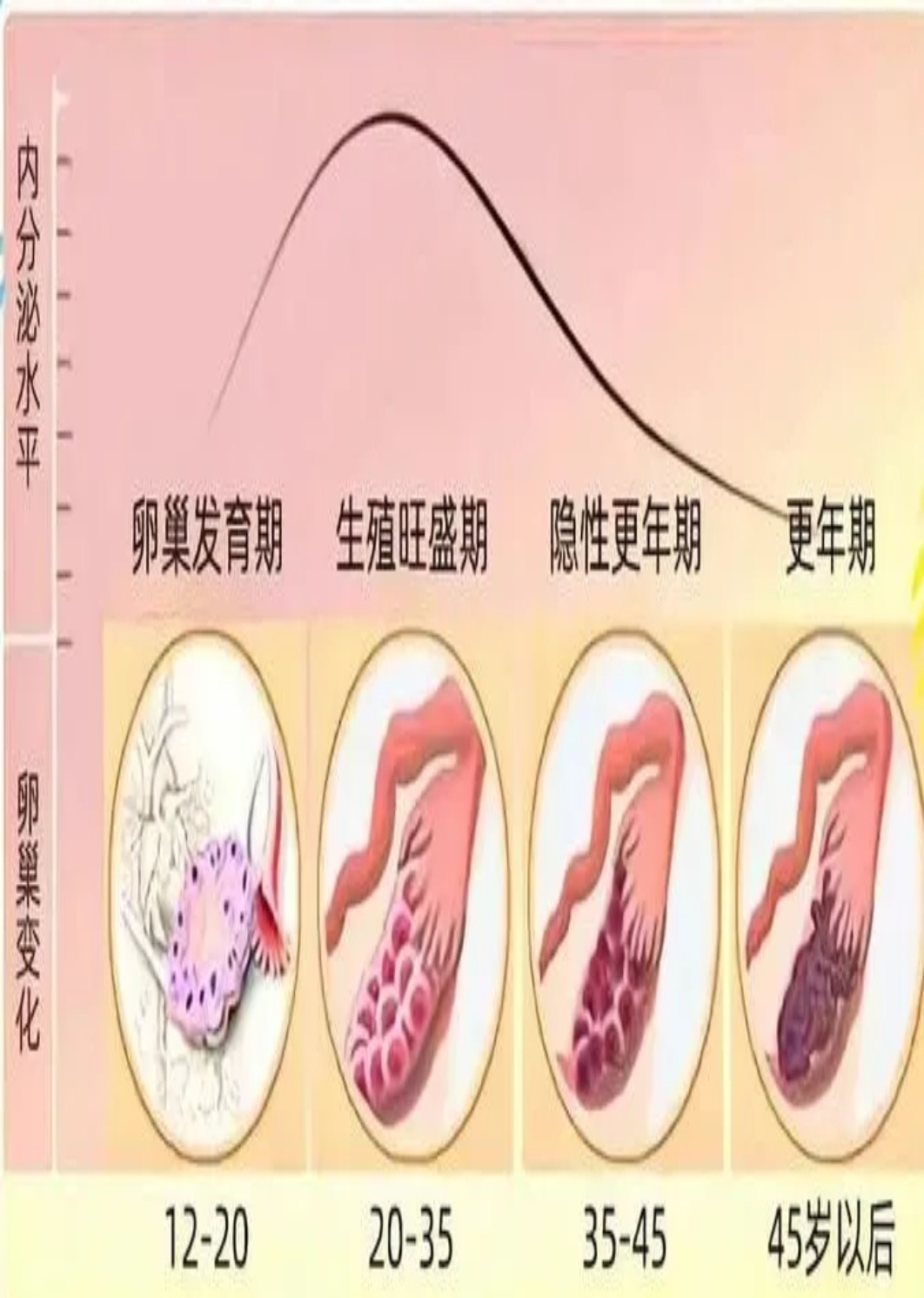
关键洞察
与年轻个体不同,中年卵巢开始依赖NAD+从头合成途径, 这一途径的衰退成为卵巢衰老的核心机制。
CD38酶介导的NAD+降解加速
CD38是近年来识别的NAD+代谢关键调控因子 [127], 其表达上调是衰老组织NAD+耗竭的"加速器"。CD38在卵巢组织中丰富表达, 且其水平与卵子质量和数量呈负相关。
恶性循环:"炎症-CD38上调-NAD+耗竭-代谢紊乱-更严重炎症"
卵母细胞线粒体功能障碍
卵母细胞线粒体具有独特的结构和功能特征: 圆形、低嵴密度、含有自身基因组但拷贝数有限(约10万-60万拷贝/卵)。 NAD+耗竭导致线粒体功能障碍表现为膜电位下降、ATP/ADP比值减小、ROS产生增加。
形态学变化:肿胀、嵴减少、基质致密化等退行性改变
2. NAD+干预对试管婴儿各阶段的影响机制与证据
2.1 卵子质量改善
卵母细胞成熟与减数分裂完成
线粒体ATP供应优化
确保纺锤体组装和染色体分离的能量需求
SIRT2酶激活
稳定纺锤体结构,降低非整倍体率
钙信号调控
维持正常的卵子激活信号传导
人类临床证据:成熟MII卵子数量增加约50%
基于112例卵巢低反应患者的自身对照研究 [114]
2.2 受精成功率提升
正常受精(双原核形成)率提高机制
精子穿透优化
ATP驱动的顶体反应和透明带穿透
卵子激活
钙振荡信号的正常传导
皮质反应
防止多精受精的屏障建立
2.3 胚胎发育质量改善
早期胚胎分裂与细胞周期调控
卵裂球对称性改善
能量供应充足减少不对称分裂,降低碎片率从25%降至15%
囊胚形成率提升
从35%提高至52%,接近年轻个体水平
滋养层细胞增殖
优化着床和胎盘发育的能量基础
A级(顶级)胚胎数量增加一倍以上
质量溢出效应:NAD+优先增强卵子和胚胎的内在能力, 而非仅仅增加数量
2.4 子宫内膜容受性与着床成功率
子宫内膜蜕膜化的能量代谢需求
子宫内膜容受性是指子宫内膜接受胚胎着床的短暂状态,其建立涉及 复杂的形态学、分子和代谢改变,统称为蜕膜化。 蜕膜化过程包括子宫内膜基质细胞的增殖、分化,血管生成, 以及免疫微环境的重塑,这些过程都对能量供应有显著需求。
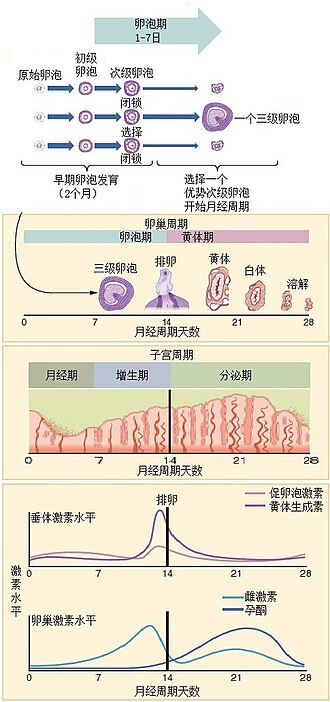
证据局限
目前关于NAD+直接改善人类子宫内膜容受性的临床证据非常有限。 主要研究聚焦于卵子获取和胚胎质量,未将着床率或临床妊娠率作为主要终点。 澳大利亚正在进行的注册临床试验将提供更可靠的数据。
3. 恩艾地注射剂(NAD+)深度分析
3.1 产品基本信息
生产企业与批准状态
生产企业
景泽生物医药(合肥)有限公司
推出企业
康诺药业
监管状态
信息透明度有待提高

信息透明度挑战
关于"恩艾地注射剂"的详细公开信息极为有限,药品批准文号、说明书、 临床试验数据等关键信息检索困难,对临床决策构成挑战。
剂型与规格特征
静脉注射剂特点
- • 分子量:663.4 Da
- • 电荷:负电荷
- • 溶解性:易溶于水
- • 稳定性:水溶液有限
核心优势
- • 近乎100%生物利用度
- • 绕过首过效应
- • 快速起效
- • 剂量准确可控
与口服制剂的差异
| 特征 | 静脉NAD+ | 口服前体 |
|---|---|---|
| 生物利用度 | ~100% | ~10-20% |
| 起效时间 | 数小时至数天 | 2-4周 |
| 首过效应 | 无 | 显著 |
| 组织分布 | 全身均衡 | 肝脏优先 |
3.2 临床使用方案
试管婴儿周期中的给药时机
促排卵前预处理(4-6周)
卵母细胞最终成熟阶段约需2-3个月
最后2-3周代谢状态对质量决定性
NAD+水平提升需要积累时间
时间紧迫情况
距离IVF >90天
口服前体150-300mg/日作为基础
距离IVF <90天
加用静脉注射快速提高血药浓度
参考方案设计
标准方案
注意事项
- • "单位"非国际通用计量
- • 不同产品间不可直接比较
- • 个体化调整必要
个体化调整依据
卵巢储备状态
AMH、AFC、既往反应
年龄因素
实际年龄、卵巢年龄
体重/BMI
分布容积影响
时间窗口
距IVF周期时间
4. NAD+补充方式的多维度比较
4.1 静脉注射NAD+(恩艾地类)
药代动力学优势
近乎100%生物利用度
静脉注射NAD+的核心药代动力学优势在于完全绕过吸收屏障, 实现剂量准确的全身分布。与口服途径相比,静脉给药避免了以下变异来源:
- • 胃肠道转运时间的个体差异
- • 肠道菌群组成的影响
- • 肠道上皮细胞摄取效率差异
- • 肝脏首过代谢的强度波动
快速起效特性
主要局限性
医疗场所依赖
经济成本考量
通常不在医保覆盖范围
4.2 口服NAD+前体
烟酰胺核苷(NR)
代谢途径
NR转化为NAD+需三步酶促反应:
临床证据
超过30项临床试验,数千名受试者安全性数据
耐受性
烟酰胺单核苷酸(NMN)
代谢途径
NMN是NAD+合成的直接前体,转化仅需两步:
发现特异性转运体SLC12A8
组织分布特征
水溶性强
稳定性较NR差,需特殊制剂
靶向组织
肝脏、骨骼肌、心脏、大脑
研究重点
主要集中在抗衰老和代谢健康领域, 动物实验中生育力改善效果最为明确
4.3 试管婴儿场景下的选择策略
时间紧迫性考量
即将进入促排周期(<8周)
时间窗口紧迫,需要快速达到有效组织浓度
推荐:静脉注射优先
- • 每周1-2次静脉输注
- • 持续4-6周
- • 可联合口服前体维持
长期备孕规划(>3个月)
时间充裕,可从容建立NAD+代谢基础
推荐:口服前体维持
- • NMN或NR 300-600mg/日
- • 持续3-6个月
- • 经济便利,可长期坚持
卵巢储备状态分层
极低储备(AMH<1)
强化静脉方案,争取最大机会
需充分告知证据局限性和费用效益比
轻度下降(AMH 1-2)
口服联合生活方式干预
平衡获益、成本和风险
联合应用方案
静脉加载+口服维持
与辅酶Q10协同
作用于线粒体电子传递链不同环节
证据基础最强,可考虑常规联合
5. 其他抗衰老干预与NAD+的协同/比较
线粒体靶向抗氧化剂
辅酶Q10(泛醇)
白藜芦醇
激素类干预
DHEA补充
生长激素
生活方式干预
热量限制/间歇性禁食
运动与睡眠优化
NAD+与其他干预的协同机制
6. 临床建议与未来展望
当前实践建议
患者知情同意要点
充分披露证据的初步性质和局限性
明确说明现有研究的方法学限制
透明讨论费用效益比和不确定性
强调个体化差异和无效可能性
监测与随访方案
周期前评估
AMH、AFC、基础FSH
周期中监测
卵泡发育同步性、雌激素曲线
实验室指标
获卵数、MII比例、胚胎质量
研究前沿与未解决问题
最佳剂量与疗程
需要系统性剂量-效应研究确定静脉NAD+的最佳单次剂量、 给药频率和疗程长度
生物标志物开发
缺乏临床可行的卵子/胚胎NAD+水平检测方法, 需要非侵入性光学检测或单细胞代谢组学技术
长期安全性随访
建立系统化的子代随访机制, 评估跨代表观遗传效应和长期健康影响
男性因素整合
目前研究几乎完全聚焦女性, 需要设计针对男性或双方联合干预的临床试验
监管与伦理考量
适应症拓展路径
与NMPA沟通
确定生殖适应症开发路径
大规模RCT
≥400例/组,主要终点活产率
药物警戒系统
上市后长期安全性监测
平衡创新与保护
NAD+处于抗衰老和生殖医学的交叉领域, 面临特殊的监管挑战和创新需求。